 Widok zawartości stron
Widok zawartości stron
 Widok zawartości stron
Widok zawartości stron
 Widok zawartości stron
Widok zawartości stron
Czym zajmuje się inżynieria tkankowa?

Z wielką przyjemnością prezentujemy zapis wykładu, jaki na inaugurację roku akademickiego 2017/18 wygłosiła dr hab. Justyna Drukała, biolog i kierownik Banku Komórek na UJ. Zapraszamy do fascynującego świata wiedzy o regeneracji komórek i narządów – przyszłości medycyny.
![]() Więcej o nauce?! Dołącz do profilu strony. www NAUKA.uj.edu.pl na Facebooku
Więcej o nauce?! Dołącz do profilu strony. www NAUKA.uj.edu.pl na Facebooku
Wykład dr hab. Justyny Drukały, koniecznie trzeba uzupełnić lekturą wywiadu z tą krakowską specjalistką inżynierii komórkowej. To rozmowa osobista, prawdziwa, szczera oraz wpisująca się w altruistyczny klimat myślenia o ludziach - tych bliskich i dalekich, tych pokrzywdzonych i tych, którym można pomóc.
O sztucznej skórze, małym Mateuszku i fascynacji nauką - wywiad z dr hab. Justyną Drukałą
Dr hab. Justyna Drukała – zajmuje się biologią komórek macierzystych, w szczególności hodowlą komórek naskórka ludzkiego do leczenia oparzeń i chronicznych owrzodzeń. Kieruje Bankiem Komórek w Zakładzie Biologii Komórki na Wydziale Biochemii, Biofizyki i Biotechnologii i w Małopolskim Centrum Biotechnologii UJ.
Jej zdaniem w pracy naukowca najważniejsza jest radość z prowadzenia badań, ale też krytyczna ocena ich wyników. „Wciąż powtarzam moim studentom" – mówi dr hab. Justyna Drukała – „że jeżeli człowiek czuje pasję, radość z tego, co robi – właśnie to w życiu powinien robić, najlepiej jak potrafi. Jak powtarzał mój mentor, profesor Włodzimierz Korohoda: »Wy się musicie bawić pracą naukową – wtedy zrobicie to dobrze«".

Regeneracja narządów jest zjawiskiem niezwykle istotnym szczególnie dla organizmów długo żyjących. Utrata ich funkcji, wywołana rozległym urazem lub chorobą, często grozi śmiercią organizmu, stąd istnieje konieczność przywrócenia prawidłowego działania uszkodzonych narządów i tkanek. Jest to jeden z zasadniczych problemów stojących przed medycyną, dlatego też na przestrzeni wieków można odnotować liczne próby jego rozwiązania.
Pierwsze wysiłki podejmowane na tym polu dotyczyły rzecz jasna mechanicznych protez. Odwołując się do historii, można dotrzeć do opisów prób zastępowania uszkodzonych części ciała różnego typu protezami. Już starożytni Egipcjanie, dla których ze względów religijnych niezwykle istotne było zachowanie integralności ciała po śmierci, dla umożliwienia rewitalizacji w życiu pozagrobowym, zwracali uwagę na konieczność zrekonstruowania ubytków w czasie balsamowania zwłok. W trakcie badań archeologicznych stwierdzono, że już około 2500 r. p.n.e. stosowano złote protezy zębowe. W Galerii Egipskiej British Museum w Londynie można obejrzeć znakomicie spreparowany sztuczny palec stopy z ok. 600 r. p.n.e. Podczas badań archeologicznych nasunęło się naukowcom pytanie, czy już wówczas protezy te nie były stosowane jednak za życia, co wskazywałoby na bardzo wczesną, błyskotliwą myśl, która dała podwaliny współczesnej protetyki.
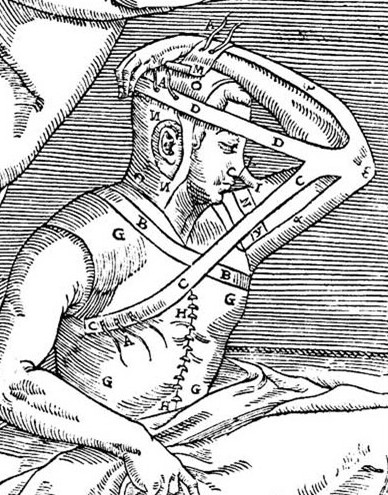
przez Gaspare Tagliacozzi, ilustracja z dzieła De Curtorum
Chirurgia per Insitionem, libri duo (1597). Źródło
Użycie różnego typu materiałów umożliwia do pewnego stopnia odtwarzanie struktury i kształtu, a także funkcji – chociaż w ograniczonym zakresie. Protezy spełniają funkcje mechaniczne, ale nie integrują się z organizmem – są do niego jedynie przymocowywane w mniej lub bardziej trwały sposób. Dla pełnej regeneracji i optymalnego odtworzenia wszystkich funkcji narządów potrzebna jest jednak żywa tkanka zawierająca komórki, elementarne jednostki życia, które tak naprawdę decydują o jej odbudowie i integracji z organizmem.
Pierwsze wzmianki dotyczące prób przeszczepienia żywych tkanek datuje się na ok. 287 r. n.e. Związane są one z postaciami świętych Kosmy i Damiana, uznawanych za patronów transplantologii. Z ich cudownymi uzdrowieniami łączy się szereg legend, a wśród nich przypowieść o cudownym przeszczepieniu dolnej kończyny, co zostało uwiecznione w ikonografii i kulcie tych świętych.
Podwaliny chirurgii plastycznej stworzył znacznie później Włoch Gaspare Tagliacozzi z Bolonii, który pod koniec XVI w. opracował i opisał metodę rekonstrukcji nosa z uszypułowanego płata skóry ramienia.
Kroki milowe
Jednak era przeszczepiania narządów sięga początku XIX w. Pierwsze udane transplantacje to wolne przeszczepy skóry w obrębie jednego pacjenta wykonane najpierw przez niemieckiego chirurga Carla Bungera w 1823 r. i 46 lat później przez Szwajcara Jacquesa Reverdin, który przeszczepiał małe wysepki skórne na trudno gojącą się ranę oraz niedługo potem Niemca Carla Thierscha, który z kolei użył do leczenia oparzenia nieco większych płatów skóry.
Przyjęcie się przeszczepionego narządu jest determinowane właściwym jego odżywianiem, o czym decyduje szybkie jego ukrwienie po wykonanej transplantacji. W tym miejscu należy przywołać nazwisko laureata Nagrody Nobla – francuskiego chirurga Alexisa Carrela, rzeczywistego twórcy transplantologii narządowej i światowego pioniera w tym zakresie, który wypracował technikę szwu chirurgicznego naczyń krwionośnych. Umożliwiło to skuteczne zespalanie naczyń przeszczepianego narządu z naczyniami biorcy i tak naprawdę otworzyło erę przeszczepów narządowych. Potwierdzeniem skuteczności tej metody były próby przeszczepu nerek w obrębie jednego osobnika.
Ciekawe? Przeczytaj również: Płodność, hormony i zdrowie. Nie ma łatwych rozwiązań
Milowym krokiem, który istotnie przyspieszył rozwój udokumentowanej transplantologii w drugiej połowie XX w., było opracowanie skutecznej anestezji, ale przede wszystkim zastosowanie immunosupresji, umożliwiającej przeszczepianie narządów od niespokrewnionych dawców. Lata 60. ubiegłego wieku obfitują w spektakularne sukcesy w transplantologii narządów. W 1967 roku po raz pierwszy skutecznie przeszczepiono serce, rok później wątrobę.
Obecnie wykonuje się już przeszczepy wielu narządów równocześnie, przeszczepia się kończyny i twarz. Również opracowanie technik i warunków przechowywania tkanek oraz narządów pobieranych od dawców pozwoliło na stworzenie banków tkanek z możliwością ich natychmiastowego wykorzystania.
Potencjał komórek macierzystych
Technika transplantacji udowodniła, że jest znaczącym sposobem osiągnięcia głównego celu całej medycyny – służenia ludzkiemu życiu. Mimo iż jest szeroko stosowana do dzisiaj i pozostaje złotym standardem w większości przypadków leczenia uszkodzeń narządów zagrażających życiu, coraz częściej napotyka się na problem dostępności dawców. Ponadto, pomimo rozwoju immunosupresji, wciąż istotną barierę stanowią powikłania związane z jej stosowaniem oraz zjawisko odrzucania przeszczepów.
Fot. Rose Spear/Flickr, licencja CC BY
Wiadomym jest, że tkanki w dojrzałym organizmie zachowują zdolność do regeneracji i dzieje się to za sprawą różnych rodzajów komórek macierzystych, które są aktywne przez całe życie organizmu. Ich liczba jest jednak niewielka, stąd w przypadku rozległych uszkodzeń, wywołanych dużym stresem (chodzi o stres w znaczeniu fizjologicznym – czyli nieprawidłowość – np. chorobę – wpływającą na ogólną kondycję organizmu – przyp. red.) , nie są one w stanie odbudować funkcjonalnej tkanki. Warto również pamiętać, że oprócz mechanizmów regeneracyjnych, które prowadzą do pełnego odtworzenia struktury i funkcji uszkodzonego narządu, natychmiast po zadziałaniu stresu równolegle aktywowane są także w organizmie inne mechanizmy naprawcze, które często pozwalają na szybkie zabezpieczenie tkanki przed dalszymi skutkami uszkodzenia, jednak doprowadzają do utworzenia blizny pozbawiającej tkankę właściwych jej funkcji.
Oczywiście komórki macierzyste, z racji swoich właściwości, od dawna były w centrum zainteresowania lekarzy i badaczy zajmującymi się procesami regeneracji tkanek i narządów. Koniec XX w. to renesans badań nad komórkami macierzystymi, możliwością ich izolacji i namnażania poza organizmem. Z drugiej strony obserwuje się w tym czasie dynamiczny rozwój różnych materiałów syntetycznych i biomateriałów stosowanych w chirurgii rekonstrukcyjnej. Stymulowany potrzebami transplantologii mariaż tych dwóch dyscyplin stanowi zaczyn nowej, bardzo dynamicznie rozwijającej się dziedziny nauki – inżynierii tkankowej, która stawia sobie za główny cel odtworzenie żywej tkanki poza organizmem.
Pionierami w tej dziedzinie są Robert Langer – amerykański biotechnolog i inżynier materiałoznawca oraz biochemik oraz Joseph Vacanti – chirurg transplantolog, którzy w 1989 roku zaproponowali definicję inżynierii tkankowej i zainspirowali burzliwy rozwój tej dziedziny nauki mieszczącej się w obszarze medycyny regeneracyjnej.
Cele, jakie stawia sobie inżynieria tkankowa, to przede wszystkim projektowanie i rozwój substytutów tkanek i narządów jako funkcjonalnej alternatywy dla konwencjonalnych przeszczepów narządowych i tkankowych.
Intensywne badania podstawowe nad możliwością hodowli komórek i tkanek in vitro są podyktowane rosnącymi potrzebami klinicznymi. Obecny stan wiedzy, a także optymalizacja technologii izolacji komórek i odtwarzania trójwymiarowej struktury tkanek pozwalają sądzić, że możliwe jest rekonstruowanie tkanek dla potrzeb klinicznych. Z tego względu istnieje rosnąca potrzeba stałego udoskonalania tych technologii i opracowania strategii ich wdrażania do klinik.
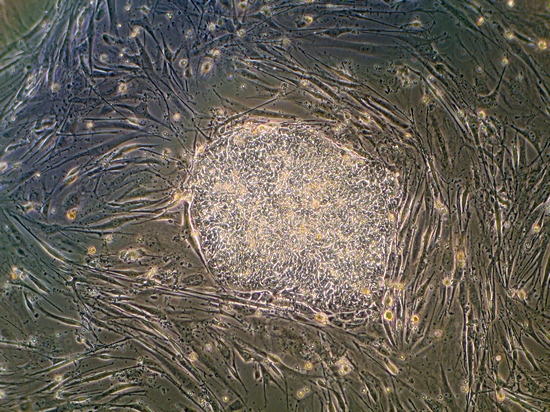
Czerpiąc wiedzę na temat budowy tkanek i narządów z badań histologicznych (dotyczących budowy tkanek – przyp. red.), a także analizując etapy tworzenia tkanek w trakcie embriogenezy, inżynieria tkankowa zakłada wykorzystanie izolowanych komórek, trójwymiarowych rusztowań – matryc, na których komórki ulegają podziałom i różnicują w celu odtworzenia oczekiwanej struktury tkanki oraz czynników sterujących procesem takiej rekonstrukcji. Jeśli chodzi o komórki, to w inżynierii tkankowej najbardziej pożądaną populacją są komórki macierzyste, bo to one decydują o regeneracji tkanek. Najbardziej plastyczne pod tym względem są embrionalne komórki macierzyste, jednak z wielu powodów nie mogą być one wykorzystane do celów terapeutycznych.
Budowanie rusztowań
Dziś już wiemy, że we wszystkich tkankach dojrzałego organizmu są obecne komórki macierzyste, natomiast ich potencjał, liczebność oraz możliwości wyizolowania i namnożenia są bardzo zróżnicowane. Optymalnym źródłem komórek są własne tkanki pacjenta, gdyż nie powodują one (niepożądanej – przyp. red.) odpowiedzi immunologicznej.
Nie zawsze jednak istnieje możliwość ich pobrania, również nie w każdym przypadku pacjent może czekać na ich namnożenie i przeszczepienie. Stąd niezależnie prowadzone są badania nad pozyskiwaniem bardziej uniwersalnych komórek macierzystych, zdolnych do regenerowania różnych tkanek.
Ciekawe? Przeczytaj także: Test Coopera, czyli ATP potrzebne na już
Poważnym przełomem w tym obszarze badań stało się nagrodzone w 2012 roku Nagrodą Nobla odkrycie Shinya Yamanaki i Johna B. Gurdona, które dowiodło, że zróżnicowane komórki pobrane z dojrzałego organizmu można tak zmodyfikować genetycznie, aby miały charakter embrionalnych komórek macierzystych. W ten sposób wskazano nowe potencjalne źródło uniwersalnych pod względem możliwości do różnicowania autologicznych komórek dla medycyny regeneracyjnej.
Jednak odtworzenie właściwej struktury narządu wiąże się nierozerwalnie z koniecznością precyzyjnego rozmieszczenia różnicujących komórek macierzystych w układzie trójwymiarowym. Czynnikiem, który to może ułatwić, jest zastosowanie odpowiednich trójwymiarowych rusztowań.
W natywnych tkankach rusztowaniem dla komórek są białka, głównie kolageny, ale także proteoglikany (patrz definicja – przyp. red.), których skład istotnie różni się w zależności od tkanki. Z jednej strony stanowią one szkielet tkanki, nadający jej specyficzne własności mechano-fizyczne, z drugiej zaś mają one wpływ na zachowanie się komórek odbudowujących tkankę, sterując licznymi procesami, które ostatecznie prowadzą do „dojrzewania tkanki” poza organizmem.
Nie zawsze istnieje możliwość pobrania komórek macierzystych, nie w każdym przypadku pacjent może też czekać na ich namnożenie i przeszczep. Stąd prowadzone są badania nad pozyskiwaniem uniwersalnych komórek macierzystych, zdolnych do regenerowania różnych tkanek.
Budulec dla tej matrycy jest produkowany i wydzielany przez komórki, stąd w inżynierii tkankowej nie ma konieczności wiernego odtwarzania składników rusztowania. W trakcie „dojrzewania tkanki” w hodowli in vitro w bioreaktorze, komórki same dokonają jego przebudowy zgodnie z jej przeznaczeniem, odpowiadając na sygnały zewnętrzne – cząsteczki regulujące funkcje komórek dostarczane w pożywce hodowlanej, w której zanurzona jest rekonstruowana żywa tkanka. Matryce mogą być wytwarzane zarówno z naturalnych biopolimerów, jak również syntetycznych, już wykorzystywanych w klinice do produkcji szwów chirurgicznych, protez, nośników leków, zastawek.
Skuteczność osadzania komórek na rusztowaniu decyduje o efektywności odtwarzania tkanki, stąd kluczowe w tym procesie jest usieciowanie rusztowania, rozmiary porów i grubość włókien, a także obecność domen rozpoznawanych przez komórki. Rusztowania wytwarzane są różnymi metodami chemicznymi i fizycznymi, natomiast ostatnio najbardziej eksplorowana jest metoda biodrukowania, która jest procesem wytwarzania trójwymiarowych struktur z rozpuszczonych składników rusztowań i żywych komórek. Biodrukowanie odbywa się na podstawie precyzyjnego modelu komputerowego generowanego na bazie tomografii komputerowej lub rezonansu magnetycznego.
Wąskim gardłem inżynierii tkankowej są rozmiary wytwarzanych poza organizmem tkanek i narządów, które nie zawierają arterii doprowadzających substancje odżywcze w głąb ich struktury. W trakcie hodowli tkanki w bioreaktorze zanurzona jest ona w pożywce, która – przy dodatkowym zastosowaniu podciśnienia – jest wtłaczana w głąb trójwymiarowej struktury tkanki, co warunkuje prawidłowe odżywianie komórek. Aby wytworzony substytut tkanki przeżył w organizmie pacjenta po implantacji, konieczne jest szybkie wniknięcie w jego strukturę naczyń krwionośnych, co warunkuje integrację z tkankami biorcy i przeżycie budujących go komórek. Idealnym rozwiązaniem, omijającym to ograniczenie, byłoby odtworzenie tkanki lub narządu z własną siecią naczyń, które podczas przeszczepu można by zespolić w miejscu przeszczepu z głównym naczyniem krwionośnym u biorcy. I takie właśnie możliwości stwarza biodrukowanie.
Samo dostarczenie komórek do miejsca uszkodzenia nie jest skutecznym rozwiązaniem, kiedy zniszczeniu uległa macierz. Wtedy również należy zapewnić regenerującej tkance rusztowanie dla prawidłowego zasiedlania jej przez komórki, które dzięki dostarczonym sygnałom podejmą różnicowanie i będą wypełniać właściwe im funkcje.
Medycyna regeneracyjna wykorzystuje wszystkie lub niektóre z wymienionych wyżej elementów tej tzw. triady inżynierii tkankowej (komórki, rusztowanie, czynniki sygnalizacyjne). W zależności od uszkodzenia tkanki jej regenerację można pobudzić dostarczając same komórki lub czynniki, które będą aktywowały pokłady uśpionych komórek macierzystych do jej odbudowy.
Sztuczna skóra na żywe rany
Skóra jest największym narządem naszego organizmu stanowiącym barierę ochronną i decydującym o utrzymaniu równowagi biologicznej. Najbardziej zewnętrzna warstwa skóry, naskórek, ma zdolność do szybkiej regeneracji za sprawą relatywnie dużej liczby komórek macierzystych w nim obecnych. Łatwość ich pozyskiwania i namnażania poza organizmem zadecydowała, iż od blisko pół wieku wykorzystuje się te komórki w leczeniu ubytków skóry i w tworzeniu bardziej skomplikowanych substytutów tego narządu. Stąd najwcześniej zaproponowane przez naukowców produkty inżynierii tkankowej to żywe odpowiedniki skóry.
W tym zakresie Bank Komórek, który dzięki inicjatywie prof. Włodzimierza Korohody powstał w Zakładzie Biologii Komórki Wydziału Biochemii, Biofizyki i Biotechnologii i działa na Uniwersytecie Jagiellońskim już od ponad 20 lat, ma istotne doświadczenie. Prowadzone są tu hodowle komórek skóry ludzkiej, które wykorzystuje się klinicznie do regeneracji rozległych ran oparzeniowych i przewlekłych ran troficznych (np. owrzodzeń – przyp. red.). W ramach projektów naukowych realizowanych we współpracy z ośrodkami klinicznymi wykonaliśmy kilkadziesiąt prób klinicznych przeczepienia komórek skóry, najwięcej we współpracy z dr. Kazimierzem Cieślikiem w Szpitalu Specjalistycznym im. L. Rydygiera oraz nieżyjącym już prof. Jackiem Puchałą w Uniwersyteckim Szpitalu Dziecięcym w Krakowie.
Niestety pokrywanie ran samymi komórkami jest skuteczne jedynie w przypadku, gdy zachowane jest dla nich naturalne rusztowanie – odpowiedniej grubości unaczyniona tkanka łączna. Stąd podejmowane są próby, również w naszym Banku, rekonstrukcji pełnej grubości skóry z wykorzystaniem komercyjnie dostępnych matryc tkankowych. W Stanach Zjednoczonych zarejestrowanych jest kilka produktów inżynierii tkankowej skóry, wśród których najbardziej zaawansowany jest Apligraf.
Obok odpowiedników skóry tkanką najczęściej regenerowaną z wykorzystaniem komórek jest chrząstka; stosowane są także produkty inżynierii tkankowej kości. Podejmowane są również liczne próby wykorzystania produktów komórkowych w leczeniu schorzeń neurologicznych. Jednocześnie prowadzone są intensywne badania i próby rekonstrukcji całych narządów, takich jak serce, wątroba czy nerka, które wciąż wymagają udoskonaleń, aby można je było skutecznie wykorzystać u człowieka.
Ciekawe? Przeczytaj także: Nieśmiertelność już za 30 lat?
Społeczne oblicze inżynierii tkankowej
Inżynieria tkankowa jest dziedziną interdyscyplinarną i tylko w takim układzie ma możliwość rozwoju w wielu płaszczyznach – od nauk podstawowych i weryfikacji na modelach zwierzęcych, poprzez próby kliniczne aż do masowej produkcji „produktów biologicznych” dopuszczonych do stosowania u pacjentów. Na podstawie badań podstawowych optymalizowane są nowe technologie i strategie leczenia, prowadzona jest również kontrola bezpieczeństwa wytwarzania produktu i jego jakości, co w konsekwencji otwiera możliwość wykorzystania produktu w praktyce klinicznej.
Ważne zadanie osób zajmujących się inżynierią tkankową stanowi zdobycie powszechnej społecznej akceptacji dla tej dziedziny medycyny oraz zainteresowanie nią sektora komercyjnego, ponieważ inżynieria tkankowa posiada niewątpliwie ogromny potencjał. Dynamiczny rozwój tej dziedziny jest jednak bardzo kosztowny, więc bez udziału kapitału przedsiębiorstw bezpośrednio zainteresowanych w wytwarzaniu takich produktów badania w tym zakresie nie są możliwe.
Dynamiczny rozwój inzynierii tkankowej jest bardzo kosztowny, więc bez udziału kapitału firm zainteresowanych w wytwarzaniu takich produktów badania nie są możliwe.
Postęp w rozwoju terapii wykorzystujących żywe komórki wymusił konieczność wprowadzenia regulacji prawnych w tym obszarze. Na terenie Unii Europejskiej obowiązuje rozporządzenie Parlamentu Europejskiego i Rady z 2007 r., 1394/2007, wdrożone ostatecznie w 2008 r. Zgodnie z tym rozporządzeniem produkty inżynierii tkankowej zostały określone jako produkty lecznicze terapii zaawansowanej. Jest to zatem nowa klasa leków, których wytwarzanie objęte jest nadzorem Ministerstwa Zdrowia i Głównego Inspektoratu Farmaceutycznego. Ich wytwarzanie może odbywać się w laboratoriach o wysokim standardzie bezpieczeństwa, zgodnie z odpowiednim systemem zapewnienia jakości, co czyni te procedury bardzo kosztownymi.
Aby nowy produkt leczniczy został wdrożony do praktyki klinicznej, musi przejść odpowiednie badania kliniczne, które potwierdzą bezpieczeństwo i skuteczność jego działania. Dopiero po tym etapie produkt taki może zostać ostatecznie zarejestrowany. W ciągu ostatnich 10 lat prowadzono ponad 1000 badań klinicznych z wykorzystaniem produktów inżynierii tkankowej w Europie, ale w tym czasie zarejestrowano tylko pięć produktów leczniczych terapii zaawansowanej.
Ostatni problem, na jaki napotyka wdrażanie produktów leczniczych terapii zaawansowanej, dość istotnie zmniejszający entuzjazm naukowców, to wysoki koszt terapii z wykorzystaniem tych produktów leczniczych, z którym wciąż nie radzi sobie ani budżet opieki zdrowotnej ani polityka zdrowotna.
Musimy jednak wciąż mieć na uwadze i mocno podkreślać, iż medycyna regeneracyjna często może być jedynym ratunkiem dla osób, które od wielu lat bezskutecznie czekają na przeszczep, straciły duże ilości tkanek wskutek wypadku, albo wycięcia guzów nowotworowych, czy też borykają się z przewlekłymi chorobami, które uniemożliwiają normalne funkcjonowanie. Wydaje się więc oczywiste, że rachunek ekonomiczny musi jednak uwzględniać możliwość skorzystania z tej szansy. Szansy, która – dzięki wspaniałemu postępowi nauki i technologii – jest w zasięgu ręki.
Na koniec należy też zaznaczyć, że zastosowanie tego typu produktów leczniczych to „terapia szyta na miarę”, ekskluzywna i dlatego jest ciągle jeszcze bardzo droga, tak jak każde zindywidualizowane podejście. Z drugiej strony, jest to idea zbyt piękna, by ludzkość nie mogła z niej nie skorzystać.
Ciekawe? Przeczytaj również: Po co nam gorączka?
Tytuł, śródtytuły i podkreślenia pochodzą od redakcji

![Dwujęzyczność – problem czy błogosławieństwo? [LangUsta cz. 2]](/documents/74541952/141538404/langusta2_230_300.jpg/ba3592d7-7d21-4421-9f11-f4c7a943f19c?t=1558386981480)
![O tym, jak mózg krojąc słowa, przyswaja nowy język [LangUsta cz. I]](/documents/74541952/141538404/langusta_300x230.jpg/d9784af1-55f4-4171-b572-d699dfeb384b?t=1555054714737)
